![]()
Traducción hecha en
la Universidad de Alcalá de Henares, España
Problemas de Energía, Enzimas y Catálisis
Tutoría del problema 5: ¿Por qué las enzimas alcanzan un máximo de velocidad para altas concentraciones de sustrato?
En la presencia de alcohol deshidrogenasa, la velocidad de reducción del acetaldehido a etanol aumenta a medida que lo hace la concentración de acetaldehido. Eventualmente la velocidad de reacción alcanza un máximo, donde posteriores aumentos de la concentración de acetaldehido no tienen efecto. ¿Por qué?
La reducción de acetaldehido a etanol es una reacción de oxidación-reducción. El acetaldehido es reducido por adición de 2 electrones y 2 protones aportados por el NADH, que resulta oxidado a NAD+.
La ecuación para esta reacción es:
| En la presencia de alcohol deshidrogenasa, la velocidad de la producción de etanol aumenta cuando la concentración de acetaldehido aumenta, como se muestra en la siguiente curva de velocidad. | 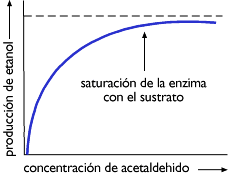 |
Una reacción catalizada por una enzima puede escribirse como:
![]()
E es la enzima, S es el sustrato (acetaldehido), ES es el complejo enzima-sustrato
y P es el producto (etanol). El sustrato se une a un lugar específico
en la superficie de la enzima, conocido como centro activo. La reacción
ocurre en la superficie de la enzima, y despues el producto y la enzima
son liberados. La enzima puede entonces unir otras moléculas de
sustrato y continuar la catálisis de la reducción del acetaldehido
muchas veces por minuto.
Una explicación de la forma de las curvas de las cinéticas enzimática
A bajas concentraciones de sustrato la velocidad de producción de etanol aumenta repentinamente con el aumento de la concentración de acetaldehido porque hay mucha enzima libre disponible (E). Para altas concentraciones de sustrato, la velocidad de la producción de etanol alcanza una meseta cuando todos los centros activos de la alcohol deshidrogenasa están saturados con sustrato (complejo ES).
Problema 5 | Respuesta | Problema
6
El Proyecto Biológico > Bioquímica > Energía, Enzimas y Catálisis
El Proyecto Biológico
Department of Biochemistry and Molecular Biophysics
University of Arizona
October 1996
Traducido: Mayo 2004
Contact the Development Team
http://www.biologia.arizona.edu
All contents copyright © 1996-2004. All rights reserved.