![]()
Traducción hecha en
la Universidad de Alcalá de Henares, España
Problemas de Energía, Enzimas y Catálisis
Tutoría del problema 3: Cinética de una enzima alostérica.
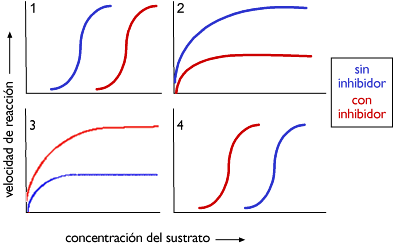
¿Cuál de las siguientes gráficas representa la velocidad de reacción frente a la concentración de sustrato para una enzima alostérica, en ausencia y presencia de un inhibidor alostérico?
Enzimas alostéricas
Las enzimas con múltiples subunidades tienen estructura cuaternaria. Una consecuencia de las subunidades múltiples es que cada subunidad catalítica individual tiene su propio centro activo. Esto significa que una enzima con estructura cuaternaria puede unir mas de una molécula de sustrato. Alostérica significa "forma diferente"; las enzimas alostéricas pueden cambiar de conformación. Las enzimas alostéricas presentan conformaciones activa e inactiva como resultado de la unión del sustrato en el centro activo y de las moléculas reguladoras en otros lugares de unión (centros alostéricos). En el caso simple de una enzima alostérica con una conformación activa y otra inactiva, el cambio en la velocidad de reacción, con el incremento de la concentración de sustrato, es tipicamente una curva con forma sigmoidea "S".Para mas información sobre enzimas alostéricas, revisar la cuestion 14 y su tutorial.
Unión de efectores a las subunidades reguladoras
Las enzimas alostéricas pueden tener también subunidades reguladoras que unen moléculas reguladoras: inhibidores o activadores. A los activadores y los inhibidores se les llama en general "efectores". Los inhibidores promueven que las enzimas alostéricas adopten su conformación inactiva y los activadores favorecen la conformación activa.Entre las dos conformaciones activa e inactiva existe un equilibrio. La cantidad de enzima activa e inactiva es dependiente de las concentraciones relativas de sustrato e inhibidor, como sugiere el siguiente diagrama:
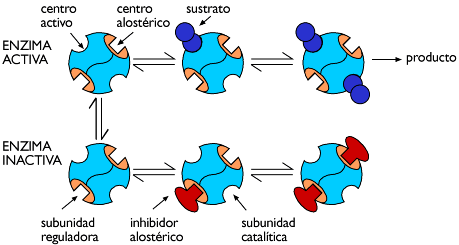
La unión de un inhibidor alostérico provoca que la enzima adopte la conformación inactiva y promueve la unión cooperativa de la segunda molécula de inhibidor.
Un exceso de sustrato puede revertir el efecto inhibidor. La unión
del sustrato promueve que la enzima asuma la conformación activa
y se favorezca la unión cooperativa de sustrato adicional, induciendo
la formación del producto.
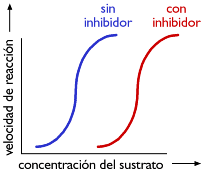
El significado de las curvas de forma-S, con y sin inhibidor
| La forma de la curva sin inhibidor esta descrita con mas detalle en
el tutorial de la cuestión 14. Cuando la concentración de
sustrato se incrementa, el sustrato se une a la enzima y dispara
el cambio de conformación hacia la conformación activa de
la enzima.
En presencia de inhibidor, se requiere mayor concentración
de sustrato para que la enzima cambie a su conformación activa.
Sin embargo, cuando se alcanza la suficiente concentración de sustrato
para disparar el cambio hacia la conformación activa, el sustrato
se une cooperativamente (curva con forma-S) y la misma velocidad máxima
se alcanza, en presencia o ausencia de inhibidor.
|
 |
Problema 3 | Respuesta | Problema 4
El Proyecto Biológico > Bioquímica > Energía, Enzimas y Catálisis
El Proyecto Biológico
Department of Biochemistry and Molecular Biophysics
University of Arizona
October 1996
Traducido: Mayo 2004
Contact the Development Team
http://www.biologia.arizona.edu
All contents copyright © 1996-2004. All rights reserved.